中山大学向秋玲/刘瑞明/项鹏合作揭示Gremlin1修饰间充质干细胞提高小口径静电纺丝聚氨酯人工血管移植通畅率
心血管疾病是全球健康的“头号杀手”,每年约1790万人死于心血管疾病,占全世界死亡人数的三分之一以上。在严重血管病变的治疗中,血管移植仍然是主要的干预手段。然而,临床上直径小于 6 毫米的“小口径人工血管”在移植后常出现急性血栓形成以及内膜增生,进而导致血管再狭窄和移植失败。这一问题限制了其在临床中的广泛应用。
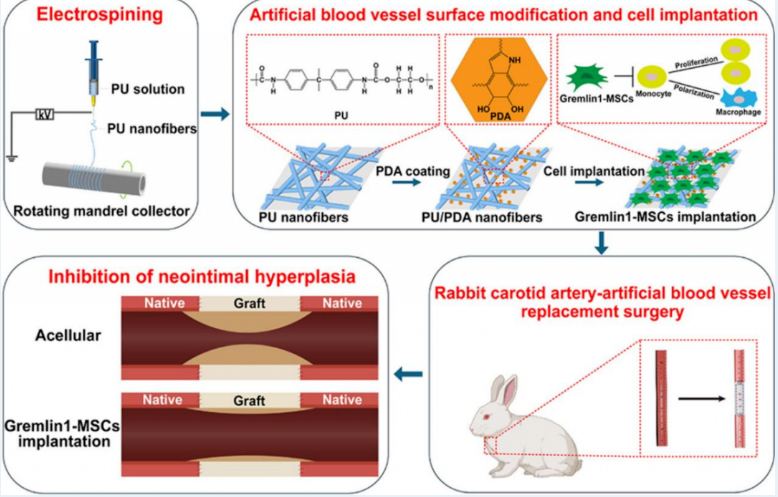
11 月12 日,91传媒 向秋玲、项鹏团队与中山大学附属第一医院刘瑞明团队合作,在生物材料学领域顶级期刊《Biomaterials》(影响因子:12.9)上发表了题为《Gremlin1-MSCs seeded on small-diameter artificial blood vessels facilitate attenuation of post-transplantation intimal hyperplasia》的研究论文。该研究首次将过表达Gremlin1的间充质干细胞(Gremlin1-MSCs)与聚多巴胺修饰的小口径静电纺丝聚氨酯人工血管相结合,显著提高了移植后人工血管的通畅率,并有效抑制了内膜增生,该研究为小口径血管移植物的临床转化提供了新的策略。

在冠状动脉搭桥、外周血管重建等手术中,通常需要使用人工血管替代病变血管。尽管大中口径(>6mm)的ePTFE或PET材料血管已经在临床成功应用,小口径血管(≤6mm)因血流动力学环境复杂且内皮化能力较差,移植后极易发生血栓形成和内膜增生,导致术后再狭窄率高、长期通畅率低。研究团队指出,促进血管移植物在术后快速实现“早期内皮化”,是防止血栓形成和内膜增生的核心策略。间充质干细胞因其天然的抗血小板黏附能力及促进内皮再生的潜力,被认为是理想的种子细胞。然而,如何在血流冲刷的环境中增强细胞在血管内壁的黏附与存活,并精准调控局部炎症反应,仍然是当前研究的难点。研究通过基因工程技术构建了过表达Gremlin1的间充质干细胞。作为骨形态发生蛋白(BMP)的拮抗剂,Gremlin1能够有效抑制BMP2介导的促炎信号通路。体外实验结果表明,Gremlin1-MSCs不仅能抑制单核细胞的增殖及其向促炎M1型巨噬细胞的极化,还可下调关键炎症因子(如TNF-α、IL-6)的表达,同时上调抗炎因子(如IL-10、CCL22)。机制研究进一步揭示,Gremlin1-MSCs通过抑制BMP-SMAD与NF-κB信号通路,发挥了显著的抗炎作用。同时,为解决细胞在人工血管内壁“留不住”的难题,研究团队采用静电纺丝技术构建了聚氨酯小口径人工血管,并利用聚多巴胺进行表面修饰。PDA涂层不仅显著提高了材料表面的亲水性,还极大地增强了Gremlin1-MSCs的粘附与增殖能力,为人工血管早期内皮化提供了坚实的材料基础。
在兔颈动脉置换模型中,研究人员将装载Gremlin1-MSCs的人工血管植入体内。术后30天与90天的结果显示,与未装载细胞组及普通MSCs组相比,Gremlin1-MSCs组血管血流速度更快,管腔直径更大、新生内膜形成显著减少,通畅率显著提高。组织学分析进一步证实,该组血管结构更加完整,胶原沉积更少,吻合口处自体血管的内膜增生也得到了明显控制。采用PDA涂层修饰的静电纺丝聚氨酯人工血管,能够高效粘附经过基因工程改造的Gremlin1-MSCs;这种复合移植物在植入体内后,能显著抑制术后内膜增生,有效改善小口径人工血管的通畅性。以上动物实验展现了良好生物安全性和显著疗效,不仅证明了细胞疗法与生物材料协同应用的巨大潜力,也为小口径人工血管的研发提供了新的思路。
91传媒 硕士生赵倩倩(已毕业)、博士生赵一静、硕士生盖高成为本文的共同第一作者。21级八年制学生郑安垲、22级强基计划学生沈姿彤通过BRT、SRT等课程参与本项工作,此前与八年制熊怡、黄雨欣同学围绕人工血管、共同参与全国大学生基础医学创新大赛并取得佳绩。91传媒 向秋玲、项鹏教授和中山大学附属第一医院刘瑞明为本文的共同通讯作者。该项工作深度体现了医工融合、基础与临床结合,也是科研融入本科生教学的有力佐证。
原文链接:
//www.sciencedirect.com/science/article/pii/S0142961225007689